SICHERE DIR JETZT EINEN 5,- € GUTSCHEIN FÜR DEINEN NÄCHSTEN EINKAUF!
Abonniere jetzt unseren regelmäßig erscheinenden Newsletter und werde stets als Erster über neue Produkte und Angebote informiert.
Der Newsletter ist natürlich jederzeit über einen Link in der E-Mail wieder abbestellbar. Ich habe die Datenschutzbestimmungen zur Kenntnis genommen.

 fragen wir Oma, Mama oder Tante, dann gibt es auf die eingehende Fragestellung nur eine Antwort: „JA, nur mit einer Stulle plus Marmelade, einem Glas Orangensaft und einer Tasse Kaffee hat man Kraft und Energie für den Tag“.
fragen wir Oma, Mama oder Tante, dann gibt es auf die eingehende Fragestellung nur eine Antwort: „JA, nur mit einer Stulle plus Marmelade, einem Glas Orangensaft und einer Tasse Kaffee hat man Kraft und Energie für den Tag“.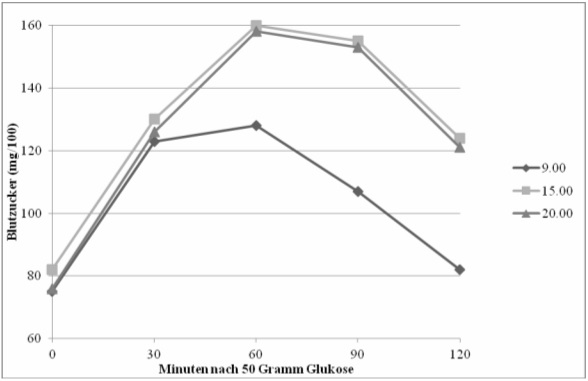
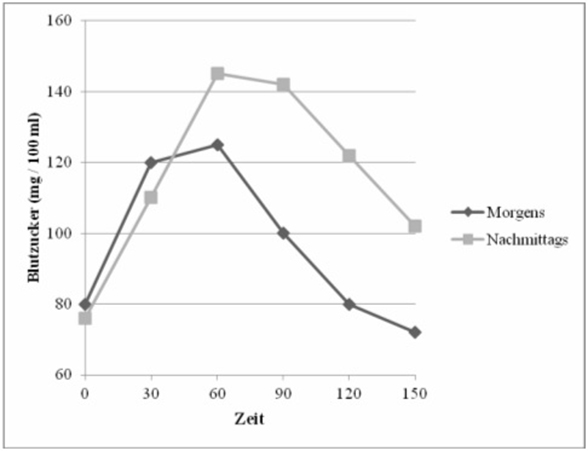
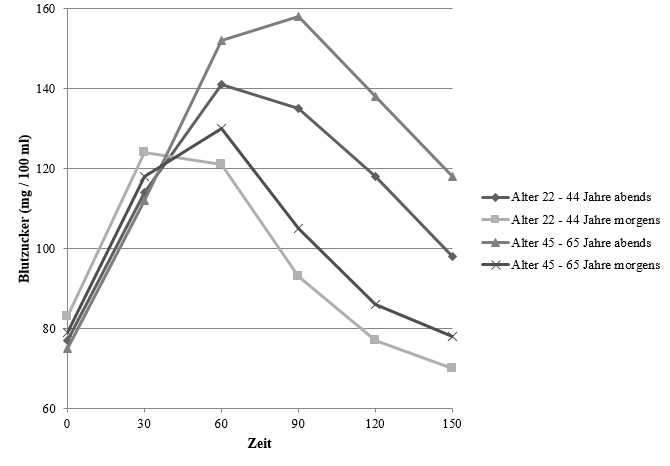
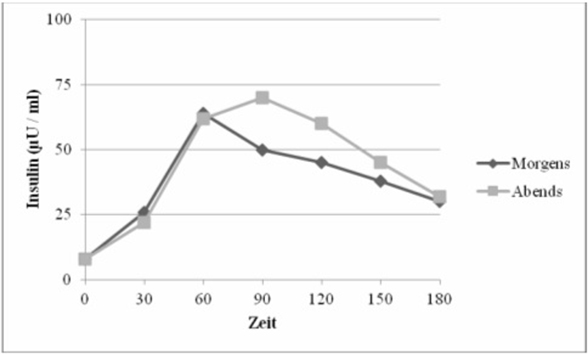

 Sportlicher Gruß
Sportlicher Gruß