Bitte wähle eine Unterkategorie
Was macht wirklich satt? – Teil 2 – Sattheit
Liebe Leserinnen und Leser, Liebe PEAK-Kundinnen und Kunden,
 Teil 1 lieferte einen Einblick in die zentrale Steuerungseinheit des Hunger- und Sättigungsgefüges. Im Rahmen der Vorstellung kurzfristiger Sättigungsgeber ließen sich bereits etliche praxisrelevante Tipps ausarbeiten, deren Umsetzung einfach ist und es ermöglicht, das Thema „Sättigung“ explizit für sich und seine Zielsetzung zu nutzen. Im heutigen Teil 2 soll es nun um Einrichtungen gehen, die sich mit einer längerfristigen Steuerung von Hunger und Sättigung befassen. Insbesondere möchte ich den stärksten aller Signalgeber, das Leptin, vorstellen.
Teil 1 lieferte einen Einblick in die zentrale Steuerungseinheit des Hunger- und Sättigungsgefüges. Im Rahmen der Vorstellung kurzfristiger Sättigungsgeber ließen sich bereits etliche praxisrelevante Tipps ausarbeiten, deren Umsetzung einfach ist und es ermöglicht, das Thema „Sättigung“ explizit für sich und seine Zielsetzung zu nutzen. Im heutigen Teil 2 soll es nun um Einrichtungen gehen, die sich mit einer längerfristigen Steuerung von Hunger und Sättigung befassen. Insbesondere möchte ich den stärksten aller Signalgeber, das Leptin, vorstellen.
Viel Spaß
Langfristige Sättigung - Sattheit
Wie lange wir zwischen Mahlzeiten satt sind (Sattheit), hängt zu einem nicht unerheblichen Teil davon ab, welche Informationen über die Höhe der Energiespeicher (Körperfettgehalt) an den Hypothalamus gesendet werden. In ihrer Gesamtheit nennt man diese Informationen „Adiposity Signals“. Sie arbeiten mit zentralnervösen orexigenen bzw. anorexigenen Signalgebern (ausführlich erklärt in Teil 3) zusammen und steuern so die langfristige Sättigung. Leptin, Amylin und Insulin zählen zu den wichtigsten und bekanntesten „Adiposity-Signals“ und sollen im Folgenden vorgestellt werden.
Interessant
Neben allen bereits genannten und noch folgenden Signalgebern gehen Melhorn et al in deren Studie mit eineiigen Zwillingen davon aus, dass die genaue Sättigungswahrnehmung auch auf erblichen Faktoren basiert. Hierbei handelt es sich um einen Faktor, den wir nicht willentlich in der Lage sind, zu beeinflussen.
Insulin
Damit unser Gehirn zur Steuerung der Energiehomöostase mit Insulin kommunizieren kann, befinden sich in einigen Hirnarealen (VMH und ARC) Andockstellen, sog. Insulinrezeptoren. Aus Studien mit direkter Verabreichung oder Abstinenz von Insulin weiß man um eine Beeinflussung der Nahrungsaufnahme und des Körpergewichts. In Verbindung mit Insulin ist es interessant zu wissen, dass es einen Unterschied zwischen dem basalen Plasmaspiegel und einem postprandialen (nach der Mahlzeit) Anstieg gibt. Ein Insulinanstieg im Gehirn ist besonders in Verbindung mit nahrungsinduzierter Insulinsekretion zu beobachten. Gerade kohlenhydratreiche Speisen erhöhen hier also den Spiegel im Gehirn mehr als dies von fettreichen Speisen zu erwarten ist. (siehe Teil 1 – Absatz Nährstoffe – Glukosensoren)
Wie es scheint, sättigen Kohlenhydrate erst einmal schlechter als die anderen beiden Makronährstoffe, sorgen jedoch nach der Mahlzeit dank postprandialem Insulinsignal für anhaltende Sattheit.
Fazit
Insulin sorgt besonders in Verbindung mit Nahrungsaufnahme und hier logischerweise insbesondere in Zusammenhang mit der Aufnahme von Kohlenhydraten für Sattheit.
Amylin
Auch Amylin stammt wie Insulin aus der Bauchspeicheldrüse und auch dieses Hormon wird insbesondere mit Erhöhung des Blutzuckers, zudem aber auch unter Anwesenheit anderer Nährstoffe ins Blut abgegeben. Wie viel Amylin gebildet wird hängt mitunter vom vorherrschenden Körperfettgehalt ab. Als hauptsächliche Wirkung des Amylins weiß man um eine Hemmung der Magenentleerung.
Fazit
Amylin und Insulin steuern zusammen mit Signalgebern für kurzfristige Signalgebung Hand in Hand den Erhalt der Energiehomöostase.
Leptin
Herkunft und Einfluss
Auf Leptin möchte ich im folgenden Abschnitt etwas näher eingehen, da es sich hierbei um das wichtigste und zugleich interessanteste „Adiposity Signal“ handelt. 167 Aminosäuren formen dieses proteinbasierte Hormon, welches größtenteils im weißen Fettgewebe gebildet wird. Bei Bedarf findet die Umwandlung von der Proform in ein bioaktives Hormon statt, welches ans Blut abgegeben und danach zur jeweiligen Zielzelle transportiert wird. Leptin hat die Eigenschaft einer Hemmung orexigener Signalgeber bzw. einer Stimulation anorexigener Signalgeber. (siehe Darstellung – Wir kommen in Teil 3 noch darauf zu sprechen). Kurz gesagt – Leptin vermittelt Sattheit.
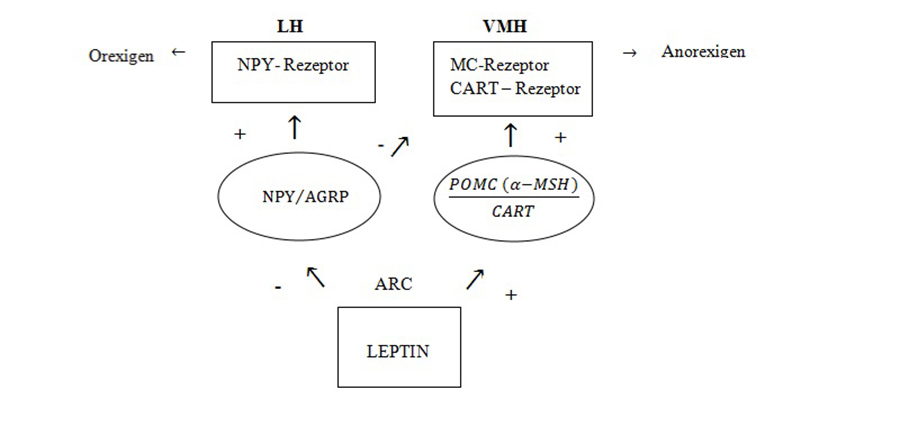 Neben der vorhandenen Rezeptorik im Gehirn (ARC und VMH) lassen sich an etlichen weiteren für den gesamten Metabolismus wichtigen Organen und Geweben Andockstellen für Leptin nachweisen wie beigefügte Darstellung zeigt.
Neben der vorhandenen Rezeptorik im Gehirn (ARC und VMH) lassen sich an etlichen weiteren für den gesamten Metabolismus wichtigen Organen und Geweben Andockstellen für Leptin nachweisen wie beigefügte Darstellung zeigt.
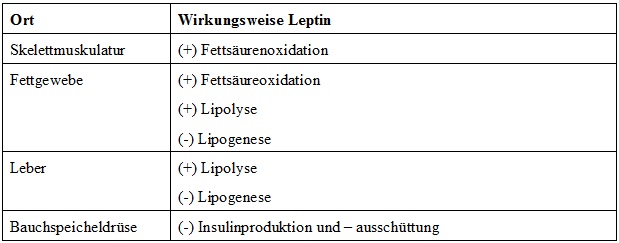
Interessant
Leptin interagiert und kommuniziert mit dem gesamten Körper, dementsprechend groß ist auch sein Einfluss.
Beeinflussung des Leptinaufkommens
Genetik
Der sog. Set-Point-Theorie von Kennedy zur Folge gibt es für jeden von uns einen Set-Point, den unser Körper in Verbindung mit Körperfett und der Leptin-Signalgebung als ausgeglichen ansieht. Je nachdem, wo sich dieser Set-Point befindet, haben es die einigen hinsichtlich Leptins und all seiner Auswirkungen einfacher, damit den Körperfettgehalt zu regulieren, während die anderen mit steigendem bzw. sinkendem Energieverbrauch oder einer Veränderung der Nahrungsaufnahme bereits Probleme in die eine oder andere Richtung bekommen. Speakman et al machen die Set-Pont-Theorie mitunter für die Existenz unterschiedlicher Körpertypen aber auch für ein unterschiedlich schnelles Auftreten einer Leptinresistenz oder aber eine mehr oder weniger ausgeprägte Reduzierung des Leptinaufkommens unter Diätbedingungen verantwortlich.
Ein gewisser Teil der Steuerung von Hunger und Sättigung via Leptin ist uns allen in die Wiege gelegt.
Körperfett
Wie viel Leptin freigesetzt wird, hängt mitunter von der Größe der Fettdepots und der metabolischen Aktivität der jeweiligen Fettzelle ab. Leptin zirkuliert einmal in einer freien und einmal in einer proteingebundenen Form. Während sich aus Untersuchungen eine direkte Korrelation zwischen der freien Form und Adipositas ableiten lässt, steht die gebundene Form Brabant et al zur Folge eher in Zusammenhang mit dem Energieverbrauch. Freies Leptin scheint dabei stärker zu sättigen als Leptin in seiner gebundenen Form.
Interessant
Adipöse Menschen weisen höhere Leptinstände auf. Ein Zustand, der sich Ahima et al zur Folge klar über das vermehrte Aufkommen an Körperfett erklären lässt. Frauen weisen generell ein höheres Aufkommen an Leptin auf als Männer. Dies begründet sich jedoch nachweislich NICHT zweifelsfrei und ausschließlich über das höhere Aufkommen an Körperfett im Verhältnis zum Körpergewicht.
Sind alle sonstigen Gegebenheiten gleich, weisen Menschen mit höherem Körperfettanteil einen höheren Leptinspiegel auf, als Personen, die einen niedrigeren Körperfettanteil verzeichnen.
Kalorienzufuhr
Studien wie die von Dubuc et al und Wisse et al zeigen, dass die Kalorienzufuhr als zweiter gewichtiger und vor allem unabhängiger Regulator für Leptin fungiert. Zwar reguliert Leptin kurzfristig nicht den Eintritt der Sättigung im Rahmen einer Mahlzeit (dies übernimmt eher Ghrelin), aber schon eine harte Diätwoche im Defizit kann das Leptinaufkommen um bis zu 50% reduzieren und damit natürlich Diätbemühungen bedeutend erschweren. Leptinmangel sorgt hier automatisch für mehr Appetit, da neben dem eigenständigen Effekt zudem Appetitanreger wie Ghrelin Neuropeptid-Y und Anandamid hochreguliert werden (das gesamte Ausmaß aller am Leptinsignal angehängter Signalgeber wird in Teil 3 nochmals verdeutlicht). Dem nicht genug kommt es leptininduziert auch zu einer reduzierten Stoffwechselrate, einem verringerten Aufkommen an Schilddrüsenhormon sowie einem messbar erhöhten Aufkommen an Cortisol.
Glücklicherweise genügen im Rahmen kalorienreduzierter Diäten schon substanzielle Erhöhungen der Kalorienzufuhr über 12 bis 24 Stunden, um den Leptinlevel wieder auf den Ausgangswert vor der Diät anzuheben, dies zeigen Kolaczynski, Weigle und Coleman in deren Untersuchungen in Verbindung mit Refeeds. Da gerade zwischen Insulin und Leptin eine enge Verbindung besteht, eignen sich besonders Kohlenhydrate für den Reset des Leptinspiegels, während Fett und Protein ohne Zugabe von Kohlenhydraten hier weit weniger effektiv zu sein scheinen.
Interessant
Seine Kohlenhydrate und damit das Insulinaufkommen im Rahmen einer Kalorienreduktion drastisch zu streichen wird sich trotz ausbleibender Blutzuckerspitzen in schier unmenschlichem Appetit bemerkbar machen. Mitunter aus diesem Grund gehören einige an den Bedarf angepasste Kohlenhydrate in jeden Diätplan.
Je länger das Kaloriendefizit, desto höher ist der Appetit ausgelöst durch weniger Leptin. Ganz gleich, ob sich der Körperfettgehalt reduziert. Gezielte Refeeds helfen!
Biorhythmus
Aus praktischer Sicht ist wichtig zu wissen, dass auch Leptin neben etlichen anderen Hormonen dem Einfluss der zirkadianen Rhythmik unterliegt, d.h. der Leptinspiegel fällt mit Verlauf des Tages unterschiedlich aus wie beigefügte Darstellung zeigt. Von Sinha erfährt man, dass diese Kurve auch für Adipöse gilt, hier fallen Verlaufs- und Spitzenwerte jedoch höher aus.
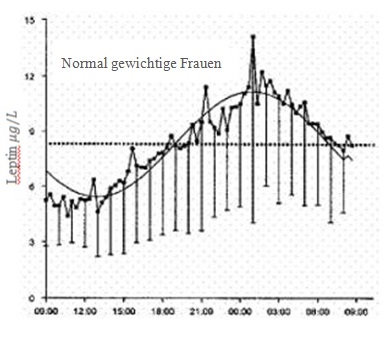
Wie es aussieht, möchte uns unser Körper mit all den zirkadianen Einflüßen etwas sagen. Morgens zeigt sich Ghrelin als Appetitanreger. Ebenfalls morgens lässt sich eine besonders gute Insulinsensivität nachweisen und Leptin signalisiert Sattheit eher nachmittags, abends und nachts. Langsam sollte auch beim letzten hier ein Lichtlein aufgehen, wann wir unserem Biorhythmus entsprechend essen sollten: „Stop Skipping Breakfast“
Weitere Infos: Ist Frühstück sinnvoll? Wir schaffen Klarheit Teil 1
Weitere Faktoren
Schlaf
Experimentelle Studien zeigten erniedrigte Spiegel an Leptin unter Schlafrestriktion. In Verbindung mit einem unter Schlafmangel zudem erhöhten Aufkommen an Ghrelin ergab sich in Studien wie denen von Knutson und Van Couver daraus ein gesteigerter Appetit. Taheri und Kollegen stellten mit regelmäßigen acht Stunden Schlaf einen um 15% höheren Leptinspiegel nach, als dieser mit nur fünf Schlafstunden nachweisbar war.
Auf genug Schlaf zu verzichten, wird sich in jedem Falle nachteilig auf das Leptinaufkommen auswirken.
Sport
Schon im Jugendlichenalter beeinflusst regelmäßige sportliche Aktivität das Leptinaufkommen. Bezogen auf die Körperfettmasse und altersspezifische Standartwerte zeigte sich bei Turnerinnen eine noch deutlichere Reduzierung als diese bei Turnern zu verzeichnen war. Auch bei Erwachsenen lassen sich derartige Effekte nachweisen. Bei Ishii et al führte 5x wöchentliches Ausdauertraining mit 50% VO2max im Rahmen einer kalorienreduzierten Diät bei Diabetikern (Typ II) zu einer Reduktion an Serumleptin um 36%. Hickey und Kollegen stellten einen solchen Effekt auch an gesunden Probanden fest, hier allerdings signifikant nur bei Frauen, während Pasman 1998 auch bei adiopösen Männern eine 23% Verringerung bei Serumleptin in Verbindung mit Sport binnen einer Interventionsdauer von 16 Monaten verzeichnete.
Gegenläufige Untersuchungen in Verbindung mit Ausdauersport gibt es von Witek (2003) und Kohort et al (1996). Während Witek aus einer Kombination mit Diät und Ausdauertraining an adipösen Frauen über 9 Wochen trotz eingetretenem Gewichtsverlust keinen eindeutigen Effekt für Ausdauertraining auf die Leptinwerte herausstellen konnte, übte Ausdauertraining auch bei Kohrt an gesunden postmenopausalen Probandinnen keinen eigenständigen Effekt auf das Leptinaufkommen aus. Eine Forschergruppe des DKFZ um Cornelia Ulrich untersuchte an 439 Probandinnen den Einfluss von Sport und/oder Ernährung auf das Leptinaufkommen. Eine starke Reduzierung des Leptinaufkommens ergab sich aus der Kombination Ernährung und Sport (40% Senkung). Der stärkste Zusammenhang wurde unabhängig vom „wie“ zwischen Leptin- und Gewichtsreduzierung festgestellt.
Spezifische Hinweise zum Leptinverhalten finden sich auch für Krafttraining. Fatouros et al testeten das Leptinverhalten an adipösen Probanden unter Verwendung unterschiedlicher Trainingsintensitäten im Rahmen eines Krafttrainingprotokolls. Wie sich herausstelle, veränderte sich das Leptinaufkommen nachhaltig (auch nach 6 Monaten noch) nur bei den Probanden mit hoher Trainingsintensität und auch nur in Verbindung mit einem Kaloriendefizit. Gippini und Kollegen verglichen das Leptinaufkommen bei Bodybuildern, mäßig übergewichtigen Nicht-Sportlern (gleicher BMI als BB) sowie schlanken Nicht-Sportlern und stellten fest, dass die mäßig übergewichtige Gruppe trotz gleichem BMI höhere Leptinwerte aufwies, während sich keine signifikanten Unterschiede zwischen Bodybuildern und schlanken Nicht-Sportlern ergaben.
Letztlich zeigen Studien wie die von Reseland oder Chu, dass sich durch Training die Leptinsensivität erhöht, was bedeutet, dass weniger Leptin notwendig ist, um ein Signal für „ausreichende Nahrungszufuhr“ zu vermitteln. Dieser ist wohl der stärkste Grund, der für Sport in Bezug auf das Leptinverhalten spricht.
Studien wie die von Cornelia Ulrich und Gippini belegen, dass Sport beim Gesunden nur ein Mittel zum Zweck, nicht aber ein starkes direktes Instrument zur Steuerung des Leptinaufkommens, darstellt. Interessanter als basale Werte ist eine via Sport mögliche Verbesserung der Leptinsensivität.
Dysregulation
Große Gefahr in Sachen Dysregulation der Sättigungssteuerung geht von einem Leptinmangel im Gehirn aus. Dieser resultiert
- aus einem echten Mangel des Hormons (genetische Störung)
- aus einer verminderten Durchlässigkeit von Leptin an der Blut-Hirnschranke
- aus einer Desensibilisierung des Leptinrezeptorsystems
- aus einem Defekt des Leptinrezeptorsystems
Interessant
Insulinsensivität und Leptinsensitivät gehen Hand in Hand. Schuld daran sind Enzyme wie SOCS3 und PTP1B, die sich sowohl in das Insulin- aber auch in das Leptinmanagement des Körpers einschalten.
Da sich die meisten der genannten Punkte aus einem falschen Lebensstil heraus ergeben, lassen sie sich Gott sei dank auch durch eine Veränderung desselben wieder ändern. Aus der Studie von Dyck aus 2004 (am Versuchstier) geht beispielsweise hervor, dass sich mit regelmäßigem Ausdauertraining Leptinresistenz über eine Reduktion des Triacylglycerinaufbaus reduzieren lässt. Ebenso wichtig (wenn nicht wichtiger) ist die Vermeidung eines Überaufkommens an Entzündungsmediatoren. Je stärker die Entzündungsneigung, desto höher die Chance auf Leptinresistenz, so zeigt es Bjorbak in seinen Studien aus 1998 und 2000.
Dysregulationen im Leptinhaushalt sind keine Seltenheit. Man begegnet diesen am besten über eine Veränderung des Lebensstils und die Vermeidung überschwelliger Entzündungsvorgänge
Resümee
Neben kurzfristigen Signalgebern (aus Teil 1) regulieren andere Einrichtungen wie Insulin und Amylin auch längerfristig das Appetitverhalten. Ein sehr wichtiger Vertreter in diesem Spiel ist das Leptin. Seine Bedeutung ergibt sich aus zahlreichen Einflüssen dank einer ausgeprägten Rezeptorik, die sich an etlichen Geweben und Organen unseres Körpers wiederfindet. Mit gezielten Maßnahmen sind wir in der Lage, nicht nur das Aufkommen an Leptin, sondern auch die Leptinsensivität zu beeinflussen.
In Teil 3 möchte ich mich mit dem letzten Puzzleteil, der bereits zitierten anorexigenen und orexigenen Effektorsysteme, befassen und nochmals die praxisrelevanten Punkte aller drei Teile zusammenfassen.
 Bis dahin verbleibe ich mit sportlichem Gruß
Bis dahin verbleibe ich mit sportlichem Gruß
Holger Gugg
www.body-coaches.de
Quellen
- Bruning JC, Gautam D, Burks DJ, Gillette J, Schubert M, Orban PC, Klein R, Krone W, Muller-Wieland D, Kahn CR. Role of brain insulin receptor in control of body weight and reproduction. Science 2000; 289: 2122–5
- Baura GD, Foster DM, Porte D, Jr., Kahn SE, Bergman RN, Cobelli C, Schwartz MW. Saturable transport of insulin from plasma into the central nervous system of dogs in vivo. A mechanism for regulated insulin delivery to the brain. J Clin Invest 1993; 92: 1824–30.
- Coleman DL, Eicher EM. Fat (fat) and tubby (tub): two autosomal recessive mutations causing obesity syndromes in the mouse. J Hered 1990; 81: 424–7.
- Kapeller R, Moriarty A, Strauss A, Stubdal H, Theriault K, Siebert E, Chickering T, Morgenstern JP, Tartaglia LA, Lillie J. Tyrosine phosphorylation of tub and its association with Src homology 2 domaincontaining proteins implicate tub in intracellular signaling by insulin. J Biol Chem 1999; 274: 24980–6.
- Arch JR. Lessons in obesity from transgenic animals. J Endocrinol Invest 2002; 25: 867–75.
- Schwartz MW, Boyko EJ, Kahn SE, Ravussin E, Bogardus C. Reduced insulin secretion: an independent predictor of body weight gain. J Clin Endocrinol Metab 1995; 80: 1571–6.
- Gerozissis K, Rouch C, Nicolaidis S, Orosco M. Brain insulin response to feeding in the rat is both macronutrient and area specific. Physiol Behav 1999; 66: 271–5.
- Reda TK, Geliebter A, Pi-Sunyer FX. Amylin, food intake, and obesity. Obes Res 2002; 10: 1087–91.
- Zhang Y, Proenca R, Maffei M, Barone M, Leopold L, Friedman JM. Positional cloning of the mouse obese gene and its human homologue. Nature 1994; 372: 425–32.
- Benoit SC, Clegg DJ, Seeley RJ, Woods SC. Insulin and leptin as adiposity signals. Recent Prog Horm Res 2004; 59: 267–85.
- Cusin I, Rohner-Jeanrenaud F, Stricker-Krongrad A, Jeanrenaud B. The weight-reducing effect of an intracerebroventricular bolus injection of leptin in genetically obese fa/fa rats. Reduced sensitivity compared with lean animals. Diabetes 1996; 45: 1446–50.
- Brabant G, Horn R, von zur Muhlen A, Mayr B, Wurster U, Heidenreich F, Schnabel D, Gruters-Kieslich A, Zimmermann-Belsing T, Feldt-Rasmussen U. Free and protein bound leptin are distinct and independently controlled factors in energy regulation. Diabetologia 2000; 43: 438–42.
- Hillebrand JJ, de Wied D, Adan RA. Neuropeptides, food intake and body weight regulation: a hypothalamic focus. Peptides 2002; 23: 2283–306.
- Woods SC, Seeley RJ, Porte D, Jr., Schwartz MW. Signals that regulatem food intake and energy homeostasis. Science 1998; 280: 1378–
- Morton GJ, Schwartz MW. The NPY/AgRP neuron and energy homeostasis. Int J Obes Relat Metab Disord 2001
- Leibel, R. L., et al., The molecular genetics of rodent single gene obesities. J. Biol. Chem. 272 (1997) 31937 - 31940.
- Barsh, G. S., et al., Genetics of boy-weight regulation. Nature 404 (2000) 644 - 651.
- Woods, A. J., Stock, M. J., Leptin activation in hypothalamus. Nature 381 (1996) 745.
- Friedman, J. M., Halaas, J. L., Leptin and the regulation of body weight in mammals. Nature 395 (1998) 763 - 770.
- Porte, D., et al., Obesity, diabetes and the central nervous system. Diabetologia 41 (1998) 863 - 881.
- Ghilardi, N., et al., Defective STAT signaling by the leptin receptor in diabetic mice. Proc. Natl. Acad. Sci. USA 93 (1996) 6231 - 6235.
- Vaisse, C., et al., Leptin activation of STAT3 in the hypothalamus of wild-type and ob/ob mice but not db/db mice. Nature Genet 14 (1996) 95 - 97.
- Schwartz, M. W., Morton G. J., Keeping hunger at bay. Nature 418 (2002) 595 - 597.
- Forbes, S., et al., Integrated control of appetite and fat metabolism by the leptin-proopiomelanocortin pathway. Proc. Natl. Acad. Sci. USA 98 (2001) 4233 - 4237.
- Korner, J., et al., Regulation of hypothalamic proopiomelanocortin by leptin in lean and obese rats. Neuroendocrinology 70 (1999) 377 - 383.
- Seeley, R. J., et al., Melanocortin receptors in leptin effects. Nature 390 (1997) 349
- Elias, C. F., et al., Leptin differentially regulates NPY and POMC neurons projecting to the lateral hypothalamic area. Neuron 23 (1999) 775 - 786.
- Cohen, P., et al., Role for stearoyl-CoA desaturase-1 in leptin-mediated weight loss. Science 297 (2002) 240 - 243.
- Ahima, R. S., et al., Leptin regulation of neuroendocrine systems. Front. Neuroendocrinol. 21 (2000) 263 - 307.
- Knutson KL , Van Cauter E. Associations between sleep loss and increased risk of obesity and diabetes.Ann N Y Acad Sci.2008; 1129: 287 – 304
- Mullington JM,Chan JL, Van Dongen HP, Szuba MP , Samaras J, Price NJ, Meier – Ewert HK,Dinges DF, Mantzoros CS .Sleep loss reduces diurnal rhythm amplitude of leptin in healthy men. J Neuroendocrinol.2003; 15: 851 – 854
- Spiegel K, Leproult R, Copinschi G, Van Cauter E. Impact of sleep length to the 24-h leptin profile. Sleep.2001; 24:abstract supplement
- Spiegel K, Tasali E, Penev P,Van Cauter E. Brief communication: Sleep curtailment in healthy young men is associated with decreased leptin levels, elevated ghrelin levels,and increased hunger and appetite.Ann Intern Med.2004; 141: 846 – 850
- https://www.dkfz.de/de/presse/pressemitteilungen/2013/dkfz-pm-13-14-Gesuendere-Hormone-durch-Ernaehrung-und-Sport.php
- Dubuc GR, Havel PJ et al. Changes of serum leptin and endocrine and metabolic parameters after 7 days of energy restriction in men and women. Metabolism. 1998 Apr;47(4):429-34.
- Klein S, et al. Leptin production during early starvation in lean and obese women. Am J Physiol Endocrinol Metab. 2000 Feb;278(2):E280-4.
- Dirlewanger M, et al. Effects of short-term carbohydrate or fat overfeeding on energy expenditure and plasma leptin concentrations in healthy female subjects. Int J Obes Relat Metab Disord. 2000 Nov;24(11):1413-8.
- Ahima RS, Flier JS. Leptin. Annu Rev Physiol. 2000;62:413-37. Review.
- Bowles L, Kopelman P. Leptin: of mice and men? J Clin Pathol 2001 Jan;54(1):1-3
- Ahima RS, et al. Leptin regulation of neuroendocrine systems. Front Neuroendocrinolgy 2000 Jul;21(3):263-307.
- van Dijk G. The role of leptin in regulation of energy balance and adiposity. J Neuroendocrinol 2001 Oct;13(10):913-21.
- Havel PJ et al. Relationship of plasma leptin to plasma insulin and adiposity in normal weight and overweight women: effects of dietary fat content and sustained weight loss. J Clin Endocrinol Metab. 1996 Dec;81(12):4406-13
- Racette SB, Kohrt WM et al. Response of serum leptin concentrations to 7 d of energy restriction in centrally obese African Americans with impaired or diabetic glucose tolerance. Am J Clin Nutr. 1997 Jul;66(1):33-7.
- Miyawaki T et al. Clinical implications of leptin and its potential humoral regulators in long-term low-calorie diet therapy for obese humans. Eur J Clin Nutr. 2002 Jul;56(7):593-600.
- Zimmet P. Serum leptin concentration, obesity, and insulin resistance in Western Samoans: cross sectional study. BMJ. 1996 Oct 19;313(7063):965-9.
- Mars M et al. Leptin and insulin responses to a four-day energy-deficient diet in men with different weight history. Int J Obes Relat Metab Disord. 2003 May;27(5):574-81.
- Pratley RE et al. Plasma leptin responses to fasting in Pima Indians. Am J Physiol. 1997 Sep;273(3 Pt 1):E644-9.
- Kolaczynski JW. Responses of leptin to short-term fasting and refeeding in humans: a link with ketogenesis but not ketones themselves. Diabetes. 1996 Nov;45(11):1511-5.
- Kolaczynski JW. Response of leptin to short-term and prolonged overfeeding in humans. J Clin Endocrinol Metab. 1996 Nov;81(11):4162-5
- van Aggel-Leijssen DP et al. Regulation of average 24h human plasma leptin level; the influence of exercise and physiological changes in energy balance. Int J Obes Relat Metab Disord. 1999 Feb;23(2):151-8.
- Girard J. Is leptin the link between obesity and insulin resistance? Diabetes Metab. 1997 Sep;23 Suppl 3:16-24. Review.
- Mars M et al. Fasting leptin and appetite responses induced by a 4-day 65%-energy-restricted diet. Int J Obes (Lond). 2006 Jan;30(1):122-8.
- Boden G et al. Effect of fasting on serum leptin in normal human subjects. J Clin Endocrinol Metab. 1996 Sep;81(9):3419-23.
- Weigle DS et al. Effect of fasting, refeeding, and dietary fat restriction on plasma leptin levels. J Clin Endocrinol Metab. 1997 Feb;82(2):561-5.
- Jenkins AB et al. Carbohydrate intake and short-term regulation of leptin in humans. Diabetologia. 1997 Mar;40(3):348-51.
- Malmstrom R et al. Insulin increases plasma leptin concentrations in normal subjects and patients with NIDDM. Diabetologia. 1996 Aug;39(8):993-6.
- Wisse BE et al. Effect of prolonged moderate and severe energy restriction and refeeding on plasma leptin concentrations in obese women. Am J Clin Nutr. 1999 Sep;70(3):321-30.
- Levine AS and CK Billington. Do circulating leptin concentrations reflect body adiposity or energy flux? Am J Cline Nutr. 1998. 68: 761-762
- Jequier E. Leptin signaling, adiposity, and energy balance. Ann N Y Acad Sci. 2002. Jun;967:379-88. Review.
- Havel, PJ. Mechanisms Regulating Leptin Production: Implications for Control of Energy Balance. American Journal of Clinical Nutrition, (Editorial) 70: 305-306, 1999.
- Kolaczynski JW. Responses of leptin to short-term fasting and refeeding in humans: a link with ketogenesis but not ketones themselves. Diabetes. 1996 Nov;45(11):1511-5.
- Weigle DS et al. Effect of fasting, refeeding, and dietary fat restriction on plasma leptin levels. J Clin Endocrinol Metab. 1997 Feb;82(2):561-5.
- Coleman RA et al. Nutritional regulation of leptin in humans. Diabetologia. 1999 42(6): 639-46
- Dirlewanger M, et al. Effects of short-term carbohydrate or fat overfeeding on energy expenditure and plasma leptin concentrations in healthy female subjects. Int J Obes Relat Metab Disord. 2000 Nov;24(11):1413-8
- Havel PJ et al. Relationship of plasma leptin to plasma insulin and adiposity in normal weight and overweight women: effects of dietary fat content and sustained weight loss. J Clin Endocrinol Metab. 1996 Dec;81(12):4406-13
- Malmstrom R et al. Insulin increases plasma leptin concentrations in normal subjects and patients with NIDDM. Diabetologia. 1996 Aug;39(8):993-6.
- Havel PJ et al. High-fat meals reduce 24-h circulating leptin concentrations in women. Diabetes. 1999 Feb;48(2):334-41
- Boden G et al. Effect of fasting on serum leptin in normal human subjects. J Clin Endocrinol Metab. 1996 Sep;81(9):3419-23.
- Carantoni M et al. Can changes in plasma insulin concentration explain the variability in leptin response to weight loss in obese women with normal glucose tolerance? J Clin Endocrinol Metab. 1999 Mar;84(3):869-72.
- Mars M et al. Leptin and insulin responses to a four-day energy-deficient diet in men with different weight history. Int J Obes Relat Metab Disord. 2003 May;27(5):574-81
- Romon M et al. Leptin response to carbohydrate or fat meal and association with subsequent satiety and energy intake. Am J Physiol. 1999 Nov;277(5 Pt 1):E855-61.
- Jenkins AB et al. Carbohydrate intake and short-term regulation of leptin in humans. Diabetologia. 1997 Mar;40(3):348-51.
- Evans et al. Carbohydrate and fat have different effects on plasma leptin concentrations and adipose tissue leptin production. Clin Sci (Lond). 2001 May;100(5):493-8.
- Havel, PJ. Peripheral signals conveying metabolic information to the brain: short-term and long-term regulation of food intake and energy homeostasis. Exp Biol Med (Maywood) 2001;226: 963-977.
- Reseland JE et al. Effect of long-term changes in diet and exercise on plasma leptin concentrations. Am J Clin Nutr. 2001 Feb;73(2):240-5.
- Chu NF et al. Dietary and lifestyle factors in relation to plasma leptin concentrations among normal weight and overweight men. Int J Obes Relat Metab Disord. 2001 Jan;25(1):106-14.
- Koutsari C et al. Plasma leptin is influenced by diet composition and exercise. Int J Obes Relat Metab Disord. 2003 Aug;27(8):901-6.
- Kondo T et al. Effect of exercise on circulating adipokine levels in obese young women. Endocr J. 2006 Apr;53(2):189-95.
- Unal M et al. Investigation of serum leptin levels and VO2max value in trained young male athletes and healthy males. Acta Physiol Hung. 2005;92(2):173-9.
- Ishigaki T et al. Plasma leptin levels of elite endurance runners after heavy endurance training. J Physiol Anthropol Appl Human Sci. 2005 Nov;24(6):573-8.
- Haluzik M et al. Effect of aerobic training in top athletes on serum leptin: comparison with healthy non-athletes. Vnitr Lek. 1999 Jan;45(1):51-4. Czech.
- Steinberg GR et al. Endurance training partially reverses dietary-induced leptin resistance in rodent skeletal muscle. Am J Physiol Endocrinol Metab. 2004 Jan;286(1):E57-63.
- Frank LL et al. Effects of exercise on metabolic risk variables in overweight postmenopausal women: a randomized clinical trial. Obes Res. 2005 Mar;13(3):615-25.
- Lakka TA et al. Leptin and leptin receptor gene polymorphisms and changes in glucose homeostasis in response to regular exercise in nondiabetic individuals: the HERITAGE family study. Diabetes. 2004 Jun;53(6):1603-8.
- Dyck DJ. Leptin sensitivity in skeletal muscle is modulated by diet and exercise. Exerc Sport Sci Rev. 2005 Oct;33(4):189-94. Review.
- Kraemer RR et al. Leptin and exercise. Exp Biol Med (Maywood). 2002 Oct;227(9):701-8. Review.
- http://www.ncbi.nlm.nih.gov/pubmed/9000710 http://www.ncbi.nlm.nih.gov/pubmed/17909627 http://www.ncbi.nlm.nih.gov/pubmed/10364187 http://www.plosone.org/article/info:doi/10.1371/journal.pone.0006884
- http://www.ncbi.nlm.nih.gov/pubmed/11797013
- http://www.ncbi.nlm.nih.gov/pubmed/11970898
- http://www.ncbi.nlm.nih.gov/pubmed/11018044 http://www.ncbi.nlm.nih.gov/pubmed/9660946
- http://www.ncbi.nlm.nih.gov/pmc/articles/PMC507189/
- http://www.ncbi.nlm.nih.gov/pubmed/11586483
- http://www.ncbi.nlm.nih.gov/pubmed/9142875
- http://www.ncbi.nlm.nih.gov/pubmed/14662513
- http://www.ncbi.nlm.nih.gov/pubmed/8923847
- http://www.plosmedicine.org/article/info:doi/10.1371/journal.pmed.0010062
- http://www.ncbi.nlm.nih.gov/pubmed/10710268
- http://www.ncbi.nlm.nih.gov/pubmed/16091494
- http://www.ncbi.nlm.nih.gov/pubmed/11018044
- http://www.ncbi.nlm.nih.gov/pubmed/9660946
- http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3064240/
- http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3209643/
Abonniere jetzt unseren regelmäßig erscheinenden Newsletter und werde stets als Erster über neue Produkte und Angebote informiert.
Der Newsletter ist natürlich jederzeit über einen Link in der E-Mail wieder abbestellbar. Ich habe die Datenschutzbestimmungen zur Kenntnis genommen.
